ДИНАМИКА НАКОПЛЕНИЯ ФЛАВОНОИДОВ В ЛИСТЬЯХ AMARANTHUS RETROFLEXUS, AGASTACHE RUGOSA И THLASPI ARVENSE СОБРАННЫХ В ЦЕНТРАЛЬНОЙ ЯКУТИИ
Аннотация
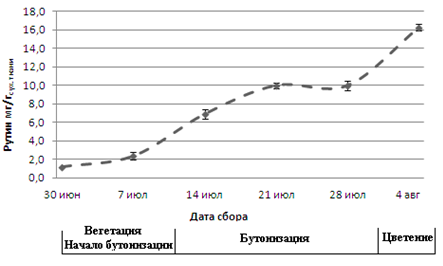
В работе исследовалось изменение содержание флавоноидов в листьях Amaranthus retroflexus, Agastache rugosa и Thlaspi arvense, собранных на территории Центральной Якутии в различные фенологические фазы. Установлено, что в листьях Amaranthus retroflexus, собранного в Центральной Якутии, содержится рутин, в листьях Agastache rugosa - лютеолин-7-О-гликозид, апигенин-7-О-гликозид, лютеолин и апигенин, а в листьях Thlaspi arvense - лютеолин-7-О-гликозид. Показано, что наибольшее содержание рутина в листьях Amaranthus retroflexus приходилось на фазу цветения. Выявлено, что максимальная концентрация лютеолин-7-О-гликозида, лютеолина и апигенина в листьях Agastache rugosa наблюдалась в период бутонизации и цветения, а апигенин-7-О-гликозида - в фазу цветения. Содержание лютеолин-7-О-гликозида в листьях Thlaspi arvense было наибольшим во время бутонизации и цветения. Таким образом, для получения растительного материала с максимальным содержанием флавоноидов у Amaranthus retroflexus, Agastache rugosa, Thlaspi arvense, выросших на территории Центральной Якутии, сбор следует проводить в период цветения.
Скачивания
Metrics
Литература
Andersen O.M., Markham K.R. Flavonoids: chemistry, biochemistry and applications. CRC Press, 2005. 1256 p.
Тараховский Ю.С., Ким Ю.А., Абдрасилов Б.С., Музафаров Е.Н. Флавоноиды: биохимия, биофизика, медицина. Пущино, 2013. 310 c.
Минаева В.Г. Флавоноиды в онтогенезе растений и их практическое использование. Новосибирск, 1978. 252 с.
Кершенгольц Б.М. Неспецифические биохимические механизмы адаптации организмов к экстремальным условиям среды // Наука и образование. 1996. Т. 3. С. 130–138.
Кершенгольц Б.М. Структурное разнообразие биологически активных веществ – биохимическая основа толерантности организмов в стрессовых условиях среды // Терпимость: идеи и традиции : материалы Международной научной конференции. Якутск, 1995. С. 179–184.
Шеин А.А., Прокопьев И.А., Филиппова Г.В., Журавская А.Н. Влияние техногенного загрязнения на содержание фотосинтетических пигментов и флавоноидов Matricaria Chamomila (Asteraceae) // Растительные ресурсы. 2014. №2. С. 235–241.
Лакин Г.Ф. Биометрия. М., 1980. 456 с.
Ломбоева С.С., Танхаева Л.М., Олейников Д.Н. Динамика накопления флавоноидов в надземной части ортилии однобокой (Orthilia Secunda (L.) House) // Химия растительного сырья. 2008. №3. С. 83–88.
Костикова В.А., Высочина Г.И., Петрук А.А. Особенности накопления флавоноидов в органах надземной части Rheum compactum L. // Химия растительного сырья. 2015. №4. С. 147–150.
Çιrak C., Radušienė J., Janulis V., Ivanauskas L. Secondary metabolites in Hypericum perfoliatum: variation among plant parts and phenological stages // Botanica Helvetica. 2007. Vol. 117. N1. Pp. 29–36.
Kazlauskas S., Bagdonaite E. Quantitative analysis of active substances in St. John's wort (Hypericum perforatum L.) by the high performance liquid chromatography method // Medicina. 2003. Vol. 40. N10. Pp. 975–981.
Kalinova J., Dadakova E. Rutin and total quercetin content in amaranth (Amaranthus spp.) // Plant foods for human nutrition. 2009. Vol. 64. N1. Pp. 68–74.
Vogelmann J.E. Flavonoids of Agastache section Agastache // Biochemical systematics and ecology. 1984. Vol. 12. N4. Pp. 363–366.
Llugany M., Tolrà R., Martín S.R., Poschenrieder C., Barceló J. Cadmium induced changes in glutathione and phenolics of Thlaspi and Noccaea species differing in Cd accumulation // Journal of Plant Nutrition and Soil Science. 2013. Vol. 176. N6. Pp. 851–858.
Formica J.V., Regelson W. Review of the biology of quercetin and related bioflavonoids // Food and chemical toxi-cology. 1995. Vol. 33. N12. Pp. 1061–1080.
Минаева В.Г., Горбалева Г.Н. О влиянии флавоноидов на прорастание пыльцы и рост пыльцевых трубок // Полезные растения природной флоры Сибири. Новосибирск, 1967. С. 231–237.
Harborne J.B., Williams C.A. Advances in flavonoid research since 1992 // Phytochemistry. 2000. Vol. 55. N6. Pp. 481–504.
Dai G.H., Nicole M., Andary C., Martinez C., Bresson E., Boher B., Daniel J.F., Geiger J.P. Flavonoids accumulate in cell walls, middle lamellae and callose-rich papillae during an incompatible interaction between Xanthomonas campestris pv. malvacearum and cotton // Physiological and Molecular Plant Pathology. 1996. Vol. 49. N5. Pp. 285–306.
Mierziak J., Kostyn K., Kulma A. Flavonoids as important molecules of plant interactions with the environment // Molecules. 2014. Vol. 19, N10. Pp. 16240–16265.

This work is licensed under a Creative Commons Attribution 4.0 International License.
Авторы, которые публикуются в данном журнале, соглашаются со следующими условиями:
1. Авторы сохраняют за собой авторские права на работу и передают журналу право первой публикации вместе с работой, одновременно лицензируя ее на условиях Creative Commons Attribution License, которая позволяет другим распространять данную работу с обязательным указанием авторства данной работы и ссылкой на оригинальную публикацию в этом журнале.
2. Авторы сохраняют право заключать отдельные, дополнительные контрактные соглашения на неэксклюзивное распространение версии работы, опубликованной этим журналом (например, разместить ее в университетском хранилище или опубликовать ее в книге), со ссылкой на оригинальную публикацию в этом журнале.
3. Авторам разрешается размещать их работу в сети Интернет (например, в университетском хранилище или на их персональном веб-сайте) до и во время процесса рассмотрения ее данным журналом, так как это может привести к продуктивному обсуждению, а также к большему количеству ссылок на данную опубликованную работу.











